Истинная регенерация. Возможна ли полная регенерация человека? Мумие для ускорения регенерации
Сейчас много говорят о выращивании отдельных органов вне организма и приращении их взамен утраченных. Но, может быть, есть способ лучше — просто восстанавливать или, выражаясь по-научному, регенерировать свои органы?
В принципе, человек отчасти наделен этим даром. Наши порезы зарастают благодаря регенерации кожи. Кровь тоже регенерируется. Но хочется большего. Причем мечтают об этом не только простые обыватели, но и ученые.
Скажем, сотрудники Лаборатории проблем регенерации Института биологии развития РАН, которой руководит доктор биологических наук Виктор Миташов, давно разрабатывает различные методы восстановления кости и нервных тканей человека, а в последнее время и сетчатки глаза. Вообще-то низшие организмы чаще способны к регенерации, чем более высокоорганизованные.
Так, среди беспозвоночных гораздо больше видов, способных восстанавливать утраченные органы, чем среди позвоночных, но лишь у некоторых из них возможна регенерация целой особи из небольшого ее фрагмента. Такие примитивные животные, как гребневики и коловратки, практически не способны к регенерации, а у гораздо более сложных ракообразных и амфибий эта способность хорошо выражена.
Многие бы хотели получит себе регенерацию как у Росомахи, героя американских комиксов. Он может за считанные минуты залечить даже самые страшные раны
Особенно удивительна способность к регенерации у губок. Ученые поставили необычный эксперимент; продавили тело взрослой губки через сетчатую ткань и отделили все образовавшиеся фрагментики друг от друга. Оказалось, что если затем поместить эти маленькие кусочки в воду и хорошенько перемешать, полностью разрушив все связи между ними, то некоторое время спустя они начнут постепенно сближаться и в конце концов воссоединятся, образовав целую губку, сходную с прежней. В этом участвует своего рода «узнавание» на клеточном уровне.
Еще один рекордсмен регенерации — ленточный червь, который способен воссоздать целую особь из любого участка своего тела. Теоретически возможно, разрезав одного червя на 200 000 кусочков, получить из него в результате регенерации столько же новых червей. А из одного луча морской звезды может возродиться целая звезда.
Но куда более известен другой пример — ящерицы, которые отращивают себе хвост, и тритоны, которые могут регенерировать глаза, лапы и хвост до шести раз.


Увы, человек этого бесценного свойства лишен. А не может ли современная наука помочь нам овладеть соответствующими механизмами?
При пересчете на жизнь человека процесс восстановления подобный тритоновскому мог бы занять у нас всего полгода. Однако разобраться до конца, каким образом тритон за месяц восстанавливает глаз, очень непросто. Ученые повторить его подвиги пока не могут. Но уже стало ясно, как он и ему подобные, это делают.
Начнем с самого начала — с рождения организма. Известно, что в ходе зародышевого развития клетки любого многоклеточного организма проходят специализацию. Из одних получаются, например, ноги, из других, скажем, мускулы, жабры или глаза. Так называемые Дох-гены дают команду как всему организму, так и конкретным органам развиваться по определенному плану — чтобы не получилось, что глаз вырастет там, где должна быть нога.
У мушки дрозофилы 8 Дох-генов, у лягушки — 6, а у человека — 38. И выяснилось, что при регенерации тритон «вспоминает» свое эмбриональное прошлое, включая генетическую программу, которая активирует Дох-гены и восстанавливает удаленные или поврежденные ткани и органы.
Но глаз или хвост должен из чего-то возникнуть — не может же он регенерироваться из воздуха. У организма есть два пути — нарабатывать новые клетки, новый строительный материал либо пользоваться тем, что осталось после утраты органа.
Выяснилось, что природа использует оба этих способа. «Кирпичами» для регенерации служат эмбриональные стволовые клетки. Так называют клетки эмбриона, которые в своем развитии просто не доросли до стадии специализации и, следовательно, способны под воздействием тех или иных факторов превратиться в клетки различных тканей и органов более чем двух сотен типов.
Причем при регенерации «старые» клетки тритона путем сложных манипуляций превращаются в сходные с эмбриональными. С ними в последнее время связано много споров. Дело в том, что для ученых главный источник эмбриональных стволовых клеток — человеческие эмбрионы. Биологи с большим энтузиазмом изучают свойства эмбриональных стволовых клеток: ведь в случае успеха эти клетки откроют совершенно новые возможности в хирургии и обеспечат восстановление тех или иных органов. Если в результате заболевания выйдут из строя какие-то группы клеток, пусть даже узкоспециализированных, то будет возможность их заменить.

И наши биологи в этих работах вовсе не на последних ролях. Скажем, академик Российской академии естественных наук Леонид Полежаев на протяжении десятилетий занимался проблемой регенерации костей свода черепа. Сначала ему удалось добиться регенерации костей черепа у собак и крыс. Затем совместно с медиками из Института нейрохирургии имени Н.Н. Бурденко АМН СССР попытались восстанавливать кости черепа у больных с травмами головы.
При этом использовались костные опилки, которые «побуждали» кости человеческого черепа к регенерации. В результате область травмы полностью закрывалась новой костью. При помощи этой методики было проведено более 250 операций.
Недавно группа ученых из Токийского университета под руководством Макото Асашимы культивировала в специальном растворе витамина А тысячи эмбриональных стволовых клеток, варьируя концентрацию витамина. Низкая концентрация активирует гены, которые контролируют развитие глазной ткани, тогда как высокая концентрация запускает работу генов, ответственных за формирование органа слуха.
Макото Асашима заявил, что таким образом целый лягушачий глаз можно получить за пять дней. Подобным, но более простым методом прежде были выращены и успешно пересажены лягушке новые почки. Животное-реципиент после этой операции прожило месяц.
А специалисты из токийского Университета Кэйо опубликовали отчет об успешном эксперименте по использованию стволовых клеток человеческого эмбриона для восстановления поврежденных тканей спинного мозга у обезьян. Как сообщил руководитель работ профессор Хидэюки Окано, исходные стволовые клетки были взяты у погибшего человеческого эмбриона с согласия родителей и одобрения университетского совета по этике.
Затем эти клетки размножили в питательной среде и подсадили пятерым обезьянам (по 10 млн клеток каждой), у которых передние конечности были обездвижены в результате травмы позвоночника. У одного примата все опорно-двигательные функции вошли в норму уже через два месяца, а у остальных процесс восстановления продолжается.
В лаборатории Виктора Миташова успешно проведены опыты по восстановлению глаза тритона. А ныне исследователи готовятся к экспериментам по выращиванию сетчатки глаза человека.
Но вот о возможности выращивания целого глаза специалисты говорят осторожно. Их можно понять: слишком велика эволюционная пропасть между тритоном и человеком. Нос другой стороны, механизмы развития органов похожи, поэтому есть надежда, что когда-нибудь биологам удастся заставить травмированного человека, «впадая в детство», выращивать нужные органы — зубы, взамен выпавших, новые клетки печени, почек, поджелудочной железы, новые мышечные ткани для сердца, пораженного инфарктом миокарда.
Способность живых организмов к регенерации органов является одной из многих таинственных загадок биологии, которую человек уже давно пытается разгадать. Еще в 2005 году всем известный журнал Science опубликовал список 25 самых важных проблем науки, в которую входит проблема раскрытия загадки регенерации органов .
Пётр Гаряев. ‹Совершенно секретно» Биология молодости
Стволовые клетки – основа регенерации
В настоящее время ученым так и не удалось до конца понять - почему же одни живеые существа, лишаясь конечности, могут быстро ее восстановить, а другие лишены такой возможности. Весь на определенном этапе развития организм знает, как это сделать, но этот этап очень короткий – срок, начинающийся и сразу заканчивающийся, когда эмбрион только начинает развиваться. В настоящее время ученые всего мира пытаются найти ответ на вопрос: можно ли разбудить это «ценное» воспоминание в мозгу взрослого человека и заставить его снова работать.
Некоторые специалисты в сфере регенеративной медицины считают, что данную функцию регенерации можно восстановить с помощью . Данные клетки в организме взрослого человека содержатся в очень маленьком количестве и располагаются в нижнем отделе позвоночника рядом с коренным узлом. Это уникальные клетки, с их помощью зарождался, а затем строился и развивался организм будущего маленького человечка.
Первые восемь клеток, образовавшиеся в результате зачатия, оплодотворения яйцеклетки сперматозоидом – это первородные стволовые клетки. Ученые выяснили, чтобы активизировать воспроизводство данных стволовых клеток нужно запустить особое вихревое поле (Мерка-ба) . Именно оно будет стимулировать активное производство стволовых клеток. При активном производстве клеток организм человека начнет регенерацию. Это и есть заветная мечта ученых регенеративной медицины.

Повреждение спинного мозга, любого органа или конечности делают из здорового активного человека инвалида на всю оставшуюся жизнь. Полностью разгадав загадку регенерации органов, ученые смогут научиться помогать таким людям, «отращивая» новые здоровые органы. Также процесс регенерации способен значительно увеличить продолжительность жизни.
Регенерация органов и тканей: как это происходит?
Целительная иммунная система саламандры
Пытаясь раскрыть тайну , ученые пристально наблюдали за организмами, которые обладают данными способностями: головастики , ящерицы , моллюски , все ракообразные , амфибии , креветки .
Особенно из данной группы ученые выделяют саламандру . Данная особь способна регенерировать, и не один раз, головной и спинной , сердце, конечности и хвост. Именно данное земноводное специалисты в области регенеративной медицины всего мира считают идеальным образцом способности регенерации.
Данный процесс у саламандры очень точный. Она может восстановить конечность полностью, но если потеряна лишь часть, то восстанавливается именно та потерянная часть. В настоящий момент точно не известно сколько же раз саламандра может восстанавливаться. Стоит отметить, что отращенная в очередной раз конечность без патологий и отклонений. Секрет данного земноводного – иммунная система , именно она помогает восстановлению органов.
Ученые очень внимательно изучают данную иммунную систему на предмет копирования методики восстановления, но уже для человеческого организма. Но пока копирование не получается, несмотря на большое количество исследований саламандры. Лишь ученые Австралийского института регенеративной медицины заявляют, что, скорее всего им удалось обнаружить основополагающий фактор способности регенерирования саламандры.

- Они утверждают, что в основе данной способности лежат клетки иммунной системы, которые предназначены для переваривания умерших клеток, грибков, бактерий, которые отторгнул организм. Ученые долго экспериментировали на саламандрах, живущих в лаборатории. Они искусственно очищали организм земноводных, тем самым «выключая» регенеративные способности. В результате на ранах просто образовывался рубец аналогичный человеческому рубцу, который появляется после серьезных травм;
- Специалисты считают, что именно клетки иммунной системы создают особые химические вещества, которые создают основу регенеративного процесса. Скорее всего, химическое вещество воспроизводится непосредственно на поврежденном участке и начинает его активно восстанавливать;
- Недавно австралийские ученые заявили, что готовят долгосрочное исследование иммунной системы человека и саламандры. Благодаря современной аппаратуре и высокому профессионализму ученых, скорее всего, в ближайшие годы будет выявлено, что именно помогает быстрой регенерации земноводных;
- Также, попутно может быть сделано открытие в сфере косметологии, протезирования и трансплантологии относительно эффективного избавления от рубцов. Данная проблема также много лет не может решиться;
- К сожалению, ни одно не обладает способностью к регенерации органов. Способность человека к регенерации можно активировать, лишь добавив в организм определенные специальные компоненты.
Исследования регенерации у млекопитающих
Однако есть специалисты, которые после долгих исследований и экспериментов, утверждают, что млекопитающие могут регенерировать кончик пальца. Данные выводы они сделали, работая с мышами . Но, степень регенерации очень ограничена. Если сравнивать лапку мыши и палец человека, то возможно отрастить утраченный фрагмент, не доходящий до места кутикулы. Если даже на миллиметр больше, то процесс регенерации уже невозможен.
Есть данные, что сообщество ученых их Японии и США смогли «разбудить» стволовые клетки мыши и отрастили большую часть конечности, равную длине среднего человеческого пальца. Они выяснили, что стволовые клетки расположены по всему телу млекопитаемого, они размножаются и становятся теми клетками, которые в данный момент наиболее нужны организму для благополучного функционирования.
Заключение
Ученые всего мира настойчиво работают, чтобы узнать с помощью чего организм человека может регенерировать органы. Если все же специалисты научатся «будить» стволовые клетки, то это будет одно из самых величайших открытий человечества. Данные знания сильно повлияют на работу абсолютно всех областей клинической медицины, позволив «заменять», в прямом смысле этого слова, негодные, мертвые органы на здоровые и эффективно восстанавливать поврежденные ткани.
В настоящее время все исследования и эксперименты проходят с обязательным участием млекопитающих и земноводных.
Общие сведения
Регенерация (от лат. regeneratio - возрождение) - восстановление (возмещение) структурных элементов ткани взамен погибших. В биологическом смысле регенерация представляет собой приспособительный процесс, выработанный в ходе эволюции и присущий всему живому. В жизнедеятельности организма каждое функциональное отправление требует затрат материального субстрата и его восстановления. Следовательно, при регенерации происходит самовоспроизведение живой материи, причем это самовоспроизведение живого отражает принцип ауторегуляции и автоматизации жизненных отправлений (Давыдовский И.В., 1969).
Регенераторное восстановление структуры может происходить на разных уровнях - молекулярном, субклеточном, клеточном, тканевом и органном, однако всегда речь идет о возмещении структуры, которая способна выполнять специализированную функцию. Регенерация - это восстановление как структуры, так и функции. Значение регенераторного процесса - в материальном обеспечении гомеостаза.
Восстановление структуры и функции может осуществляться с помощью клеточных или внутриклеточных гиперпластических процессов. На этом основании различают клеточную и внутриклеточную формы регенерации (Саркисов Д.С., 1977). Для клеточной формы регенерации характерно размножение клеток митотическим и амитотическим путем, для внутриклеточной формы, которая может быть органоидной и внутриорганоидной, - увеличение числа (гиперплазия) и размеров (гипертрофия) ультраструктур (ядра, ядрышек, митохондрий, рибосом, пластинчатого комплекса и т.д.) и их компонентов (см. рис. 5, 11, 15). Внутриклеточная форма регенерации является универсальной, так как она свойственна всем органам и тканям. Однако структурно-функциональная специализация органов и тканей в фило- и онтогенезе «отобрала» для одних преимущественно клеточнуую форму, для других - преимущественно или исключительно внутриклеточную, для третьих - в равной мере обе формы регенерации (табл. 5). Преобладание той или иной формы регенерации в определенных органах и тканях определяется их функциональным назначением, структурно-функциональной специализацией. Необходимость сохранения целостности покровов тела объясняет, например, преобладание клеточной формы регенерации эпителия как кожи, так и слизистых оболочек. Специализированная функция пирамидной клетки головного
мозга, как и мышечной клетки сердца, исключает возможность деления этих клеток и позволяет понять необходимость отбора в фило- и онтогенезе внутриклеточной регенерации как единственной формы восстановления данного субстрата.
Таблица 5. Формы регенерации в органах и тканях млекопитающих (по Саркисову Д.С., 1988)
Эти данные опровергают существовавшие до недавнего времени представления об утрате некоторыми органами и тканями млекопитающих способности к регенерации, о «плохо» и «хорошо» регенерирующих тканях человека, о том, что существует «закон обратной зависимости» между степенью дифференцировки тканей и способностью их к регенерации. В настоящее время установлено, что в ходе эволюции способность к регенерации в некоторых тканях и органах не исчезла, а приняла формы (клеточную или внутриклеточную), соответствующие их структурному и функциональному своеобразию (Саркисов Д.С., 1977). Таким образом, все ткани и органы обладают способностью к регенерации, различны лишь ее формы в зависимости от структурно-функциональной специализации ткани или органа.
Морфогенез регенераторного процесса складывается из двух фаз - пролиферации и дифференцировки. Особенно хорошо эти фазы выражены при клеточной форме регенерации. В фазу пролиферации размножаются молодые, недифференцированные клетки. Эти клетки называют камбиальными (от лат. cambium - обмен, смена), стволовыми клетками и клетками-предшественниками.
Для каждой ткани характерны свои камбиальные клетки, которые отличаются степенью пролиферативной активности и специализации, однако одна стволовая клетка может быть родоначальником нескольких видов
клеток (например, стволовая клетка кроветворной системы, лимфоидной ткани, некоторые клеточные представители соединительной ткани).
В фазу дифференцировки молодые клетки созревают, происходит их структурно-функциональная специализация. Та же смена гиперплазии ультраструктур их дифференцировкой (созреванием) лежит в основе механизма внутриклеточной регенерации.
Регуляция регенераторного процесса. Среди регуляторных механизмов регенерации различают гуморальные, иммунологические, нервные, функциональные.
Гуморальные механизмы реализуются как в клетках поврежденных органов и тканей (внутритканевые и внутриклеточные регуляторы), так и за их пределами (гормоны, поэтины, медиаторы, факторы роста и др.). К гуморальным регуляторам относят кейлоны (от греч. chalaino - ослаблять) - вещества, способные подавлять деление клеток и синтез ДНК; они обладают тканевой специфичностью. Иммунологические механизмы регуляции связаны с «регенерационной информацией», переносимой лимфоцитами. В связи с этим следует заметить, что механизмы иммунологического гомеостаза определяют и структурный гомеостаз. Нервные механизмы регенераторных процессов связаны прежде всего с трофической функцией нервной системы, а функциональные механизмы - с функциональным «запросом» органа, ткани, который рассматривается как стимул к регенерации.
Развитие регенераторного процесса во многом зависит от ряда общих и местных условий, или факторов. К общим следует отнести возраст, конституцию, характер питания, состояние обмена и кроветворения, к местным - состояние иннервации, крово- и лимфообращения ткани, пролиферативную активность ее клеток, характер патологического процесса.
Классификация. Различают три вида регенерации: физиологическую, репаративную и патологическую.
Физиологическая регенерация совершается в течение всей жизни и характеризуется постоянным обновлением клеток, волокнистых структур, основного вещества соединительной ткани. Нет таких структур, которые не подвергались бы физиологической регенерации. Там, где доминирует клеточная форма регенерации, имеет место обновление клеток. Так происходит постоянная смена покровного эпителия кожи и слизистых оболочек, секреторного эпителия экзокринных желез, клеток, выстилающих серозные и синовиальные оболочки, клеточных элементов соединительной ткани, эритроцитов, лейкоцитов и тромбоцитов крови и т.д. В тканях и органах, где клеточная форма регенерации утрачена, например в сердце, головном мозге, происходит обновление внутриклеточных структур. Наряду с обновлением клеток и субклеточных структур постоянно совершается биохимическая регенерация, т.е. обновление молекулярного состава всех компонентов тела.
Репаративная или восстановительная регенерация наблюдается при различных патологических процессах, ведущих к повреждению клеток и тка-
ней. Механизмы репаративной и физиологической регенерации едины, репаративная регенерация - это усиленная физиологическая регенерация. Однако в связи с тем, что репаративная регенерация побуждается патологическими процессами, она имеет качественные морфологические отличия от физиологической. Репаративная регенерация может быть полной и неполной.
Полная регенерация, или реституция, характеризуется возмещением дефекта тканью, которая идентична погибшей. Она развивается преимущественно в тканях, где преобладает клеточная регенерация. Так, в соединительной ткани, костях, коже и слизистых оболочках даже относительно крупные дефекты органа могут путем деления клеток замещаться тканью, идентичной погибшей. При неполной регенерации, или субституции, дефект замещается соединительной тканью, рубцом. Субституция характерна для органов и тканей, в которых преобладает внутриклеточная форма регенерации, либо она сочетается с клеточной регенерацией. Поскольку при регенерации происходит восстановление структуры, способной к выполнению специализированной функции, смысл неполной регенерации не в замещении дефекта рубцом, а в компенсаторной гиперплазии элементов оставшейся специализированной ткани, масса которой увеличивается, т.е. происходит гипертрофия ткани.
При неполной регенерации, т.е. заживлении ткани рубцом, возникает гипертрофия как выражение регенераторного процесса, поэтому ее называют регенерационной, в ней - биологический смысл репаративной регенерации. Регенераторная гипертрофия может осуществляться двумя путями - с помощью гиперплазии клеток или гиперплазии и гипертрофии клеточных ультраструктур, т.е. гипертрофии клеток.
Восстановление исходной массы органа и его функции за счет преимущественно гиперплазии клеток происходит при регенерационной гипертрофии печени, почек, поджелудочной железы, надпочечников, легких, селезенки и др. Регенерационная гипертрофия за счет гиперплазии клеточных ультраструктур характерна для миокарда, головного мозга, т.е. тех органов, где преобладает внутриклеточная форма регенерации. В миокарде, например, по периферии рубца, заместившего инфаркт, размеры мышечных волокон значительно увеличиваются, т.е. они гипертрофируются в связи с гиперплазией их субклеточных элементов (рис. 81). Оба пути регенерационной гипертрофии не исключают друг друга, а, наоборот, нередко сочетаются. Так, при регенерационной гипертрофии печени происходит не только увеличение числа клеток в сохранившейся после повреждения части органа, но и гипертрофия их, обусловленная гиперплазией ультраструктур. Нельзя исключить того, что в мышце сердца регенерационная гипертрофия может протекать не только в виде гипертрофии волокон, но и путем увеличения числа составляющих их мышечных клеток.
Восстановительный период обычно не ограничивается только тем, что в поврежденном органе развертывается репаративная регенерация. Если
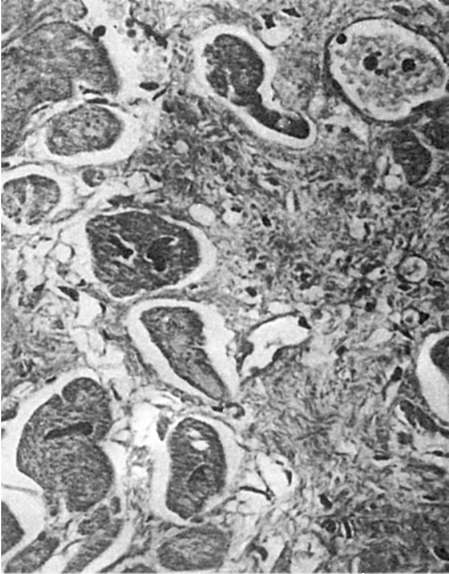 Рис. 81.
Регенерационная гипертрофия миокарда. По периферии рубца расположены гипертрофированные мышечные волокна
Рис. 81.
Регенерационная гипертрофия миокарда. По периферии рубца расположены гипертрофированные мышечные волокна
воздействие патогенного фактора прекращается до гибели клетки, происходит постепенное восстановление поврежденных органелл. Следовательно, проявления репаративной реакции должны быть расширены за счет включения восстановительных внутриклеточных процессов в дистрофически измененных органах. Общепринятое мнение о регенерации только как о завершающем этапе патологического процесса малооправданно. Репаративная регенерация не местная, а общая реакция организма, охватывающая различные органы, но реализующаяся в полной мере лишь в том или ином из них.
О патологической регенерации говорят в тех случаях, когда в результате тех или иных причин имеется извращение регенераторного процесса, нарушение смены фаз пролиферации
и дифференцировки. Патологическая регенерация проявляется в избыточном или недостаточном образовании регенерирующей ткани (гипер- или гипорегенерация), а также в превращении в ходе регенерации одного вида ткани в другой [метаплазия - см. Процессы приспособления (адаптации) и компенсации]. Примерами могут служить гиперпродукция соединительной ткани с образованием келоида, избыточная регенерация периферических нервов и избыточное образование костной мозоли при срастании перелома, вялое заживление ран и метаплазия эпителия в очаге хронического воспаления. Патологическая регенерация обычно развивается при нарушениях общих и местных условий регенерации (нарушение иннервации, белковое и витаминное голодание, хроническое воспаление и т.д.).
Регенерация отдельных тканей и органов
Репаративная регенерация крови отличается от физиологической прежде всего своей большей интенсивностью. При этом активный красный костный мозг появляется в длинных трубчатых костях на месте жирового костного мозга (миелоидное превращение жирового костного мозга). Жировые клетки вытесняются растущими островками кроветворной ткани, которая заполняет костномозговой канал и выглядит сочной, темнокрасной. Кроме того, кроветворение начинает происходить вне костного мозга - внекостномозговое, или экстрамедуллярное, кроветворение. Оча-
ги экстрамедуллярного (гетеротопического) кроветворения в результате выселения из костного мозга стволовых клеток появляются во многих органах и тканях - селезенке, печени, лимфатических узлах, слизистых оболочках, жировой клетчатке и т.д.
Регенерация крови может быть резко угнетена (например, при лучевой болезни, апластической анемии, алейкии, агранулоцитозе) или извращена (например, при злокачественной анемии, полицитемии, лейкозе). В кровь при этом поступают незрелые, функционально неполноценные и быстро разрушающиеся форменные элементы. В таких случаях говорят о патологической регенерации крови.
Репаративные возможности органов кроветворной и иммунокомпетентной системы неоднозначны. Костный мозг обладает очень высокими пластическими свойствами и может восстанавливаться даже при значительных повреждениях. Лимфатические узлы хорошо регенерируют только в тех случаях, когда сохраняются связи приносящих и выносящих лимфатических сосудов с окружающей их соединительной тканью. Регенерация ткани селезенки при повреждении бывает, как правило, неполной, погибшая ткань замещается рубцом.
Регенерация кровеносных и лимфатических сосудов протекает неоднозначно в зависимости от их калибра.
Микрососуды обладают большей способностью регенерировать, чем крупные сосуды. Новообразование микрососудов может происходить путем почкования или аутогенно. При регенерации сосудов путем почкования (рис. 82) в их стенке появляются боковые выпячивания за счет усиленно делящихся эндотелиальных клеток (ангиобласты). Образуются тяжи из эндотелия, в которых возникают просветы и в них поступает кровь или лимфа из «материнского» сосуда. Другие элементы: сосудистой стенки образуются за счет дифференцировки эндотелия и окружающих сосуд соединительнотканных клеток, В сосудистую стенку врастают нервные волокна из предсуществующих нервов. Аутогенное новообразование сосудов состоит в том, что в соединительной ткани появляются очаги недифференцированных клеток. В этих очагах возникают щели, в которые открываются предсуществующие капилляры и изливается кровь. Молодые клетки соединительной ткани, дифференцируясь, образуют эндотелиальную выстилку и другие элементы стенки сосуда.
 Рис. 82.
Регенерация сосудов путем почкования
Рис. 82.
Регенерация сосудов путем почкования
Крупные сосуды не обладают достаточными пластическими свойствами. Поэтому при повреждении их стенки восстанавливаются лишь структуры внутренней оболочки, ее эндотелиальная выстилка; элементы средней и наружной оболочек обычно замещаются соединительной тканью, что ведет нередко к сужению или облитерации просвета сосуда.
Регенерация соединительной ткани начинается с пролиферации молодых мезенхимальных элементов и новообразования микрососудов. Образуется молодая, богатая клетками и тонкостенными сосудами соединительная ткань, которая имеет характерный вид. Это - сочная темнокрасная ткань с зернистой, как бы усыпанной крупными гранулами поверхностью, что явилось основанием назвать ее грануляционной тканью. Гранулы представляют собой выступающие над поверхностью петли новообразованных тонкостенных сосудов, которые составляют основу грануляционной ткани. Между сосудами много недифференцированных лимфоцитоподобных клеток соединительной ткани, лейкоцитов, плазматических клеток и лаброцитов (рис. 83). В дальнейшем происходит созревание грануляционной ткани, в основе которой лежит дифференцировка клеточных элементов, волокнистых структур, а также сосудов. Число гематогенных элементов уменьшается, а фибробластов - увеличивается. В связи с синтезом фибробластами коллагена в межклеточных пространствах образуются аргирофильные (см. рис. 83), а затем и коллагеновые волокна. Синтез фибробластами гликозаминогликанов служит образованию
основного вещества соединительной ткани. По мере созревания фибробластов количество коллагеновых волокон увеличивается, они группируются в пучки; одновременно уменьшается количество сосудов, они дифференцируются в артерии и вены. Созревание грануляционной ткани завершается образованием грубоволокнистой рубцовой ткани.
Новообразование соединительной ткани происходит не только при ее повреждении, но и при неполной регенерации других тканей, а также при организации (инкапсуляции), заживлении ран, продуктивном воспалении.
Созревание грануляционной ткани может иметь те или иные отклонения. Воспаление, развивающееся в грануляционной ткани, приводит к задержке ее созревания,
 Рис. 83.
Грануляционная
ткань. Между тонкостенными сосудами много недифференцированных клеток
соединительной ткани и аргирофильных волокон. Импрегнация серебром
Рис. 83.
Грануляционная
ткань. Между тонкостенными сосудами много недифференцированных клеток
соединительной ткани и аргирофильных волокон. Импрегнация серебром
а чрезмерная синтетическая активность фибробластов - к избыточному образованию коллагеновых волокон с последующим резко выраженным их гиалинозом. В таких случаях возникает рубцовая ткань в виде опухолевидного образования синюшно-красного цвета, которая возвышается над поверхностью кожи в виде келоида. Келоидные рубцы образуются после различных травматических поражений кожи, особенно после ожогов.
Регенерация жировой ткани происходит за счет новообразования соединительнотканных клеток, которые превращаются в жировые (адипозоциты) путем накопления в цитоплазме липидов. Жировые клетки складываются в дольки, между которыми располагаются соединительнотканные прослойки с сосудами и нервами. Регенерация жировой ткани может происходить также из ядросодержащих остатков цитоплазмы жировых клеток.
Регенерация костной ткани при переломе костей в значительной мере зависит от степени разрушения кости, правильной репозиции костных отломков, местных условий (состояние кровообращения, воспаление и т.д.). При неосложненном костном переломе, когда костные отломки неподвижны, может происходить первичное костное сращение (рис. 84). Оно начинается с врастания в область дефекта и гематомы между отломками кости молодых мезенхимальных элементов и сосудов. Возникает так называемая предварительная соединительнотканная мозоль, в которой сразу же начинается образование кости. Оно связано с активацией и пролиферацией остеобластов в зоне повреждения, но прежде всего в периостате и эндостате. В остеогенной фиброретикулярной ткани появляются малообызвествленные костные балочки, число которых нарастает.
Образуется предварительная костная мозоль. В дальнейшем она созревает и превращается в зрелую пластинчатую кость - так образуется
 Рис. 84.
Первичное костное сращение. Интермедиарная костная мозоль (показана стрелкой), спаивающая отломки кости (по Г.И. Лаврищевой)
Рис. 84.
Первичное костное сращение. Интермедиарная костная мозоль (показана стрелкой), спаивающая отломки кости (по Г.И. Лаврищевой)
окончательная костная мозоль, которая по своему строению отличается от костной ткани лишь беспорядочным расположением костных перекладин. После того как кость начинает выполнять свою функцию и появляется статическая нагрузка, вновь образованная ткань с помощью остеокластов и остеобластов подвергается перестройке, появляется костный мозг, восстанавливаются васкуляризация и иннервация. При нарушении местных условий регенерации кости (расстройство кровообращения), подвижности отломков, обширных диафизарных переломах происходит вторичное костное сращение (рис. 85). Для этого вида костного сращения характерно образование между костными отломками сначала хрящевой ткани, на основе которой строится костная ткань. Поэтому при вторичном костном сращении говорят о предварительной костно-хрящевой мозоли, которая со временем превращается в зрелую кость. Вторичное костное сращение по сравнению с первичным встречается значительно чаще и занимает больше времени.
При неблагоприятных условиях регенерация костной ткани может быть нарушена. Так, при инфицировании раны регенерация кости задерживается. Костные осколки, которые при нормальном течении регенераторного процесса выполняют функцию каркаса для новообразованной костной ткани, в условиях нагноения раны поддерживают воспаление, что тормозит регенерацию. Иногда первичная костно-хрящевая мозоль не дифференцируется в костную. В этих случаях концы сломанной кости остаются подвижными, образуется ложный сустав. Избыточная продукция костной ткани в ходе регенерации приводит к появлению костных выростов - экзостозов.
Регенерация хрящевой ткани в отличие от костной происходит обычно неполно. Лишь небольшие дефекты ее могут замещаться новообразованной тканью за счет камбиальных элементов надхрящницы - хондробластов. Эти клетки создают основное вещество хряща, затем превращаются в зрелые хрящевые клетки. Крупные дефекты хряща замещаются рубцовой тканью.
Регенерация мышечной ткани, ее возможности и формы различны в зависимости от вида этой ткани. Гладкие мьшщы, клетки которых обладают способностью к митозу и амитозу, при незначительных дефектах могут регенерировать достаточно полно. Значительные участки повреждения гладких мышц замещаются рубцом, при этом сохранившиеся мышечные волокна подвергаются гипертрофии. Новообразование гладких мышечных волокон может происходить путем превращения (метаплазии) элементов соединительной ткани. Так образуются пучки гладких мышечных волокон в плевральных спайках, в подвергающихся организации тромбах, в сосудах при их дифференцировке.
Поперечнополосатые мышцы регенерируют лишь при сохранении сарколеммы. Внутри трубок из сарколеммы осуществляется регенерация ее органелл, в результате чего появляются клетки, называемые миобластами. Они вытягиваются, число ядер в них увеличивается, в саркоплазме
 Рис. 85.
Вторичное костное сращение (по Г.И. Лаврищевой):
Рис. 85.
Вторичное костное сращение (по Г.И. Лаврищевой):
а - костно-хрящевая периостальная мозоль; участок костной ткани среди хрящевой (микроскопическая картина); б - периостальная костно-хрящевая мозоль (гистотопограмма через 2 мес после операции): 1 - костная часть; 2 - хрящевая часть; 3 - отломки кости; в - периостальная мозоль, спаивающая смещенные отломки кости
дифференцируются миофибриллы, и трубки сарколеммы превращаются в поперечнополосатые мышечные волокна. Регенерация скелетных мышц может быть связана и с клетками-сателлитами, которые располагаются под сарколеммой, т.е. внутри мышечного волокна, и являются камбиальными. В случае травмы клетки-сателлиты начинают усиленно делиться, затем подвергаются дифференцировке и обеспечивают восстановление мышечных волокон. Если при повреждении мышцы целость волокон нарушается, то на концах их разрывов возникают колбообразные выбухания, которые содержат большое число ядер и называются мышечными почками. При этом восстановления непрерывности волокон не происходит. Место разрыва заполняется грануляционной тканью, превращающейся в рубец (мышечная мозоль). Регенерация мышцы сердца при ее повреждении, как и при повреждении поперечнополосатой мускулатуры, заканчивается рубцеванием дефекта. Однако в сохранившихся мышечных волокнах происходит интенсивная гиперплазия ультраструктур, что ведет к гипертрофии волокон и восстановлению функции органа (см. рис. 81).
Регенерация эпителия осуществляется в большинстве случаев достаточно полно, так как он обладает высокой регенераторной способностью. Особенно хорошо регенерирует покровный эпителий. Восстановление многослойного плоского ороговевающего эпителия возможно даже при довольно крупных дефектах кожи. При регенерации эпидермиса в краях дефекта происходит усиленное размножение клеток зародышевого (камбиального), росткового (мальпигиева) слоя. Образующиеся эпителиальные клетки сначала покрывают дефект одним слоем. В дальнейшем пласт эпителия становится многослойным, клетки его дифференцируются, и он приобретает все признаки эпидермиса, включающего в себя ростковый, зернистый блестящий (на подошвах и ладонной поверхности кистей) и роговой слои. При нарушении регенерации эпителия кожи образуются незаживающие язвы, нередко с разрастанием в их краях атипичного эпителия, что может послужить основой для развития рака кожи.
Покровный эпителий слизистых оболочек (многослойный плоский неороговевающий, переходный, однослойный призматический и многоядерный мерцательный) регенерирует таким же образом, как и многослойный плоский ороговевающий. Дефект слизистой оболочки восстанавливается за счет пролиферации клеток, выстилающих крипты и выводные протоки желез. Недифференцированные уплощенные клетки эпителия сначала покрывают дефект тонким слоем (рис. 86), затем клетки принимают форму, свойственную клеточным структурам соответствующей эпителиальной выстилки. Параллельно частично или полностью восстанавливаются и железы слизистой оболочки (например, трубчатые железы кишки, железы эндометрия).
Регенерация мезотелия брюшины, плевры и околосердечной сумки осуществляется путем деления сохранившихся клеток. На поверхности дефекта появляются сравнительно крупные кубические клетки, которые затем уплощаются. При небольших дефектах мезотелиальная выстилка восстанавливается быстро и полно.
Важное значение для восстановления покровного эпителия и мезотелия имеет состояние подлежащей соединительной ткани, так как эпителизация любого дефекта возможна лишь после заполнения его грануляционной тканью.
Регенерация специализированного эпителия органов (печени, поджелудочной железы, почек, желез внутренней секреции, легочных альвеол) осуществляется по типу регенерационной гипертрофии: в участках повреждения ткань замещается рубцом, а по периферии его происходят гиперплазия и гипертрофия клеток паренхимы. В печени участок некроза всегда подвергается рубцеванию, однако в остальной части органа происходит интенсивное новообразование клеток, а также гиперплазия внутриклеточных стуктур, что сопровождается их гипертрофией. В результате этого исходная масса и функция органа быстро восстанавливаются. Регенераторные возможности печени почти безграничны. В поджелудочной железе регенераторные процессы хорошо выражены как в экзокринных отделах, так и в панкреатических островках, причем эпителий экзокринных желез становится источником восстановления островков. В почках при некрозе эпителия канальцев происходит размножение сохранившихся нефроцитов и восстановление канальцев, однако лишь при сохранении тубулярной базальной мембраны. При ее разрушении (тубулорексис) эпителий не восстанавливается и каналец замещается соединительной тканью. Не восстанавливается погибший канальцевый эпителий и в том случае, когда одновременно с канальцем погибает сосудистый клубочек. При этом на месте погибшего нефрона разрастается рубцовая соединительная ткань, а окружающие нефроны подвергаются регенерационной гипертрофии. В железах внутренней секреции восстановительные процессы также представлены неполной регенерацией. В легком после удаления отдельных долей в оставшейся части происходит гипертрофия и гиперплазия тканевых элементов. Регенерация специализированного эпителия органов может протекать атипично, что ведет к разрастанию соединительной ткани, структурной перестройке и деформации органов; в таких случаях говорят о циррозе (цирроз печени, нефроцирроз, пневмоцирроз).
Регенерация разных отделов нервной системы происходит неоднозначно. В головном и спинном мозге новообразования ганглиозных клеток не про-
 Рис. 86.
Регенерация эпителия в дне хронической язвы желудка
Рис. 86.
Регенерация эпителия в дне хронической язвы желудка
исходит и при разрушении их восстановление функции возможно лишь за счет внутриклеточной регенерации сохранившихся клеток. Невроглии, особенно микроглии, свойственна клеточная форма регенерации, поэтому дефекты ткани головного и спинного мозга обычно заполняются пролиферирующими клетками невроглии - возникают так называемые глиальные (глиозные) рубцы. При повреждении вегетативных узлов наряду с гиперплазией ультраструктур клеток происходит и их новообразование. При нарушении целости периферического нерва регенерация происходит за счет центрального отрезка, сохранившего связь с клеткой, в то время как периферический отрезок погибает. Размножающиеся клетки шванновской оболочки погибшего периферического отрезка нерва располагаются вдоль него и образуют футляр - так называемый бюнгнеровский тяж, в который врастают регенерирующие осевые цилиндры из проксимального отрезка. Регенерация нервных волокон завершается их миелинизацией и восстановлением нервных окончаний. Регенерационная гиперплазия рецепторов, перицеллюлярных синаптических приборов и эффекторов иногда сопровождается гипертрофией их концевых аппаратов. Если регенерация нерва в силу тех или иных причин нарушается (значительное расхождение частей нерва, развитие воспалительного процесса), то в месте его перерыва образуется рубец, в котором беспорядочно располагаются регенерировавшие осевые цилиндры проксимального отрезка нерва. Аналогичные разрастания возникают на концах перерезанных нервов в культе конечности после ее ампутации. Такие разрастания, образованные нервными волокнами и фиброзной тканью, называются ампутационными невромами.
Заживление ран
Заживление ран протекает по законам репаративной регенерации. Темпы заживления ран, его исходы зависят от степени и глубины раневого повреждения, структурных особенностей органа, общего состояния организма, применяемых методов лечения. По И.В. Давыдовскому, выделяют следующие виды заживления ран: 1) непосредственное закрытие дефекта эпителиального покрова; 2) заживление под струпом; 3) заживление раны первичным натяжением; 4) заживление раны вторичным натяжением, или заживление раны через нагноение.
Непосредственное закрытие дефекта эпителиального покрова - это простейшее заживление, заключающееся в наползании эпителия нд поверхностный дефект и закрытии его эпителиальным слоем. Наблюдаемое на роговице, слизистых оболочках заживление под струпом касается мелких дефектов, на поверхности которых быстро возникает подсыхающая корочка (струп) из свернувшейся крови и лимфы; эпидермис восстанавливается под корочкой, которая отпадает через 3-5 сут после ранения.
Заживление первичным натяжением (per rimamm intentionem) наблюдается в ранах с повреждением не только кожи, но и подлежащей ткани,
причем края раны ровные. Рана заполняется свертками излившейся крови, что предохраняет края раны от дегидратации и инфекции. Под влиянием протеолитических ферментов неитрофилов происходит частичный лизис свертка крови, тканевого детрита. Нейтрофилы погибают, на смену им приходят макрофаги, которые фагоцитируют эритроциты, остатки поврежденной ткани; в краях раны обнаруживается гемосидерин. Часть содержимого раны удаляется в первый день ранения вместе с экссудатом самостоятельно или при обработке раны - первичное очищение. На 2-3-и сутки в краях раны появляются растущие навстречу друг другу фибробласты и новообразованные капилляры, появляется грануляционная ткань, пласт которой при первичном натяжении не достигает больших размеров. К 10-15-м суткам она полностью созревает, раневой дефект эпителизируется и рана заживает нежным рубчиком. В хирургической ране заживление первичным натяжением ускоряется в связи с тем, что ее края стягиваются нитями шелка или кетгута, вокруг которых скапливаются рассасывающие их гигантские клетки инородных тел, не мешающие заживлению.
Заживление вторичным натяжением (per secundam intentionem), или заживление через нагноение (или заживление посредством гранулирования - per granulationem), наблюдается обычно при обширных ранениях, сопровождающихся размозжением и омертвением тканей, проникновении в рану инородных тел, микробов. На месте раны возникают кровоизлияния, травматический отек краев раны, быстро появляются признаки демаркационного гнойного воспаления на границе с омертвевшей тканью, расплавление некротических масс. В течение первых 5-6 сут происходит отторжение некротических масс - вторичное очищение раны, и в краях раны начинает развиваться грануляционная ткань. Грануляционная ткань, выполняющая рану, состоит из 6 переходящих друг в друга слоев (Аничков Н.Н., 1951): поверхностный лейкоцитарно-некротический слой; поверхностный слой сосудистых петель, слой вертикальных сосудов, созревающий слой, слой горизонально расположенных фибробластов, фиброзный слой. Созревание грануляционной ткани при заживлении раны вторичным натяжением сопровождается регенерацией эпителия. Однако при этом виде заживления раны на месте ее всегда образуется рубец.
Что такое регенерация и как она происходит? Ответы на данные вопросы имеются частично. К примеру, ученые уже знают, что такое регенерация. Данный процесс всячески испытывали в лабораторных условиях, но так и не смогли полностью определить, как и почему она происходит у некоторых видов. В данной статье мы разберемся с этим понятием и попробуем определить, свойственна ли регенерация человеку.
Кто в процессе эволюции освоил регенерацию
Регенерацией называют процесс восстановления. Некоторые существа могут восстанавливать утраченные конечности и некоторые органы. Например, тритоны (их считают одними из самых древних на нашей планете) могут отрастить себе новый хвост, лапу и даже челюсть. Это действительно уникальное существо, относящееся к хвостатым амфибиям.
После длительного изучения тритонов в лабораториях всего мира, ученые определили, что у них регенерируются не только утраченные конечности, но и жизненно важные органы: сердечные ткани, глаза, спинной мозг. Благодаря уникальности тритоны бывают в космосе чаще собак и обезьян. У них имеется феноменальная способность «приспосабливаться».
Еще регенерацию в процессе эволюции освоили рыбки «данио рерио», которых мы часто держим в домашних аквариумах. Эти красивые существа небольшого размера умеют восстанавливать сердце, плавники, глаза. Исследователи специально вырезали рыбкам вышеперечисленные органы, после чего те их сравнительно быстро восстанавливали. К слову, другие виды рыб тоже так умеют, но зачастую быстро восстанавливают только плавники.

К классическим примерам регенерации относятся:
- ящерицы и головастики, которые отращивают новые хвосты (в детстве практически каждый отрывал нечаянно ящерице хвост, после чего родители убеждали, что у нее отрастет новый);
- крабы и прочие ракообразные, способные восстанавливать клешни – основное свое «оружие»;
- улитки, которые отращивают новые «рожки»;
- саламандры, умеющие регенерировать отрезанные конечности;
- морские звезды, отращивающие себе новые «лучи» (своеобразные конечности).
Чемпион регенерации

Чемпионом в данном деле принято считать червя «плосковика» либо «планарию». Если это существо разрезать на две равные половины, то на одно половине регенерируется недостающий хвост, а на другой – недостающая голова. Организм червя как-то понимает, что ему необходимо отрастить. Если на переднем и заднем концах этого существа произвести небольшие разрезы, то у него отрастут вторые хвост и голова. Самое интересное, что даже из 1/280 части тела «плосковика» получится самостоятельное, полностью развитое, здоровое живое существо.
История изучения регенерации
Ученых всегда интересовало, как животные научились регенерировать утраченные части тело. Человеку тоже не помешала бы такая возможность. Специалисты в различных отраслях науки проводили эксперименты, чтобы вывести законы данного сверхъестественного навыка.
Первым, кто вплотную подошел к изучению регенерации, был француз Р. А. Реомюр. Именно он придумал термин «регенерация» и стал использовать его. В 1712 году опубликовали его первую работу, связанную с регенерацией конечностей у ракообразных. Коллеги скептически восприняли труды Реомюра, из-за чего у ученого пропало желание дальше заниматься изучением регенерации.
Феноменальной способностью снова заинтересовались спустя 30 лет. Опыты продолжил А. Трабле. Именно он обнаружил самое загадочное существо, способное регенерировать, и проводил на нем опыты (речь идет о «плосковике», описанном выше). Ученый долго не мог определить, на ком он экспериментирует. Существо выглядело как пустой внутри стебель с щупальцами и присоской, которой оно прикреплялось к стенке аквариума. Позже оказалось, что в руках у Абраама находился хищник, причем очень интересный.

Отдельные фрагменты тела подопытного быстро превращались в нового полноценного хищника. На месте разрезов отрастали новые части тела, из-за чего существо становилось похожим на фантастического монстра. Трабле назвал существо «гидрой».
Опыты Трабле не остались без внимания. Шокированные ученые пытались повторить их на всем, что шевелилось. Вскоре в мире появилась целая группа живых существ, способных восстанавливаться. На протяжении нескольких десятилетий в нее входили только простейшие организмы, но потом ученые узнали, что птицы могут отращивать новый клюв, а крысы – отрезанный хвост.
Благодаря чему организмы могут регенерироваться?

Ученые обнаружили, что если тритон, например, потеряет конечность, то на поврежденном участке клетки различных тканей теряют признаки отличия. Вторично рожденные клетки называют теперь «бластемой». Их особенностью является ускоренное и усиленное деление. Эти «бластемы» определяют свое предназначение в зависимости от того, какой части тела они нужнее.
На регенерацию можно воздействовать. Ученые выяснили, что если во время восстановления лапки лягушки воздействовать на новорожденные вторично клетки кислотой витамина А, то вместо одной конечности у лягушки вырастет несколько. К слову, опыты на хладнокровных проводятся потому, что вышеописанный навык развит лучше всего именно у них. Почему-то теплокровные не научили восстанавливать значительные участки тела.
Регенерация у человека

Как известно, человек не может отрастить себе новую конечность. Но регенерировать его организм все-таки умеет. Простейшей регенерацией можно назвать заживление раны и тому подобное. Человек не может полноценно восстанавливать утраченные конечности по нескольким причинам.
Доктор наук в области биологии Петр Гаряев считает, что умение регенерировать у нас ослабилось во время эволюции, так как человек всегда был более защищенным от внешних воздействий, чем остальные живые существа. Мы обладаем завидной выносливостью, можем быстро находить выход из любой ситуации, легко приспосабливаемся к новым условиям. Из-за этого полная регенерация нам не нужна. Она сохранилась у нас частично, благодаря чему растут ногти и волосы, заживают раны, восстанавливается обожженная либо ободранная кожа.
Можно ли заставить организм человека регенерировать

Вернемся к «бластеме». Если бы у человека имелись такие клетки, то теоретически он мог бы регенерировать свои конечности и все прочее, что могут восстанавливать хладнокровные. В человеческом организме имеется два вида клеток, способных регенерировать. Это клетки крови и печени.
Во время развития эмбриона часть клеток воздерживаются от специализации. Эти клетки называются стволовыми. Именно они могут пополнять запасы крови и восстанавливать ткани печени, при необходимости. Стволовые клетки, находящиеся в костном мозгу, могут превращаться в мышцы, ткани, кости или хрящи. Благодаря этому их можно назвать своеобразной «бластемой».
Ученые уже пытаются проверить опытным путем, можно ли в человеке развить способность регенерировать большие участки тела с помощью программирования стволовых клеток. Для этого они берут данные клетки и воздействуют на них определенным образом в лабораторных условиях, пытаясь заставить видоизменяться в нужном направлении. Более того, у ученых уже получается выращивать органы из стволовых клеток. Осталось только научиться выращивать полноразмерные органы, способные самостоятельно функционировать. Именно с этим возникают проблемы.
Дело в том, что то, что удается крошечному организму, очень сложно осуществить большому человеческому. Теоретически мы можем поступить как тритоны: регенерировать маленькую ручку или ножку, после чего выращивать ее. Но тритонам на это требуется не больше месяца, а нам – около 20-и лет.
К слову, добывать вышеописанные клетки очень сложно и дорого. Такие клетки в максимальном количестве находятся в костном мозге тазовых костей, но у взрослого человека стволовые клетки теряют свою функциональность. Самыми перспективными считаются стволовые клетки, полученные из пуповинной крови. После родов можно собрать около 50 мл такой крови. Из каждого миллилитра можно получить всего 1 миллион стволовых клеток, и только 1% из них оказываются подходящими для регенерации. Поэтому, чтобы развить человеческую регенерацию ученым придется научиться создавать стволовые клетки в лаборатории или заставить другие органы человеческого тела вырабатывать их. К счастью, наука не стоит на месте. Возможно, когда-нибудь человек научится восстанавливаться подобно тритону или даже «плосковику».
Регенерация. Общие положения. Виды регенерации. Репаративная и патологическая регенерация. Заживление повреждений. Организация и перестройка тканей. Адаптация и компенсация: определение понятий, уровни и виды (морфо-функциональный резерв, системная интеграция органов, гиперплазия и гипертрофия). Декомпенсация. Атрофия. Перестройка органов и тканей.
1) РЕГЕНЕРАЦИЯ - постоянно происходящий в живом организме процесс восстановления клеток и межклеточного вещества взамен утрачиваемых в ходе физиологической их деградации. В результате регенерации структура и функция органов и тканей поддерживается на нормальном уровне.
Классификация регенераторных процессов.
1. Физиологическая регенерация (постоянно происходит в норме)
2. Репаративная регенерация - имеет место при патологических процессах и заболеваниях, сопровождающихся значительными тканевыми повреждениями. Бывает полной и неполной. Полная регенерация - restitutio ad integrum.
Неполная регенерация - substitutio, представляет собой перестройку пораженного органа или ткани с организацией зоны повреждения. Репаративная регенерация является синонимом заживления.
3. ПАТОЛОГИЧЕСКАЯ РЕГЕНЕРАЦИЯ - гипорегенерация, гиперрегенерация (гипертрофические разрастания), дисплазия. (Дисплазия - как пример извращенной адаптации в патологии - дизадаптация).
Дисплазия - обратимый клеточный и тканевой атипизм; при значительной степени выраженности может выступать в качестве предрака.
Физиологическая и репаративная регенерация осуществляется на внутриклеточном и клеточном уровнях. На внутриклеточном уровне регенерация представлена новообразованием ультраструктур, на клеточном - восстановлением количества клеток путем их деления. Внутриклеточная регенерация ультраструктур является основным и самым древним механизмом восстановления структуры и функции клеток. Она присуща всем органам и тканям. Клеточная регенерация осуществляется путем восстановления исходного количества клеток за счёт деления камбиальнах клеток. Такой путь регенерации имеется в эпителиальной выстилке кожных покровов и слизистых оболочек, кроветворной, лимфоидной и костной тканях. Напротив, в кардиомиоцитах и нейронах центральной нервной системы в ответ на гибель соответствующих клеток восстановление функции осуществляется только за счёт усиленной внутриклеточной регенерации в оставшихся клетках, которые берут на себя нагрузку, приходившуюся на погибшие клетки. Деления клеток при этом в обычных условиях не происходит. Сохранению функциональной активности на должном уровне в таких органах также способствует наличие большого клеточного резерва (90% нейронов в ЦНС). В таких органах, как печень, почки регенерация может осуществляться обеими путями - внутриклеточным и клеточным.
Конкретный тип регенерации определяется морфо-функциональной специализацией органа или ткани и полностью подчинен особенностям их функционирования. Регенерация соединительной ткани осуществляется посредством размножения её клеточных элементов и новообразования капилляров. В результате формируется молодая соединительная ткань, называемая г р а н у л я ц и о н н о й т к а н ь ю. По мере её созревания фибробласты, соединительнотканные волокна и капилляры принимают продольное направление соответственно направлению механических нагрузок.
2) ЗАЖИВЛЕНИЕ (регенерация) ПОВРЕЖДЕНИЙ. В основе этого процесса лежат регенерация тканей с их организацией и перестройкой (см. ниже).
Различают п о л н о е заживление и н е п о л н о е заживление. Полное заживление (restitutio ad integrum) является синонимом полной репаративной регенерации. Полное заживление имеется в случаях незначительного повреждения эпителиальных тканей, когда дефект замещается размножающимися эпителиальными клетками (клеточная форма регенерации). При этом возможны 2 варианта полного заживления: непосредственное закрытие дефекта путём наползания на него эпителиального покрова и заживление под струпом (корочка из свернувшейся крови и лимфы).
Неполное заживление (substitutio)-синоним неполной репаративной регенерации, которая сопровождается образованием более или менее выраженного соединительнотканного рубца. Неполное заживление имеет место при значительных тканевых повреждениях, захватывающих строму органа или подлежащую соединительную ткань, а также при повреждениях органов, где клеточное деление паренхиматозных элементов не возможно (мышцы, миокард, нервная система). Неполное заживление кожных покровов и слизистых оболочек может протекать по типу заживления первичным натяжением и заживления вторичным натяжением. Заживление первичным натяжением происходит в тех случаях, когда края раны ровные, без размозжения, не инфицированы. При этом происходит образование небольшого количества грануляционной ткани, сращение краёв раны осуществляется в короткие сроки
5-7 дней, а полное заживление с эпителизацией поверхности наступает на 15 сутки. Если же края раны с широкой зоной некроза, рана инфицирована и загрязнена посторонними частицами, то заживлению предшествует длительный период нагноения с образованием обильных грануляций и в последующем грубых деформирующих рубцов. Такой вариант заживления является нежелательным, поэтому для создания условий для заживления открытых ран первичным натяжением применяется первичная хирургическая обработка ран с удалением скальпелем некротизированных тканей, удалением инородных частиц, промыванием раны антисептиками и наложением первичных швов.
4) АДАПТАЦИЯ (или приспособление) - широкое биологическое понятие, отражающее способность организма приспосабливаться к изменившимся условиям внешней и внутренней среды и являющееся неотъемлемым свойством живого организма или популяции организмов. Адаптация способствует сохранению жизни индивида (особи) и в конечном итоге всей популяции. Адаптация происходит в норме и в патологии. В норме адаптивные процессы представлены регенерацией, перестройкой, включением морфо-функциональных резервов и системной интеграцией
органов и тканей. При этом адаптивные процессы осуществляют приспосабливаемость организма в пределах физиологических колебаний нагрузок. Адаптивные процессы в патологии называются компенсацией (или компенсаторными процессами).
5) КОМПЕНСАЦИЯ - совокупность морфологических изменений в клетках, тканях или органах, направленных на восстановление и усиление их функции при заболеваниях. Компенсаторные процессы представлены: а) включением структурно-функционального резерва, б) внутриклеточной и клеточной гиперплазией, в) клеточной и внутриклеточной гипертрофией, г) метаплазией, д) системной интеграцией морфо-функциональных структур с образованием временных функциональных систем. Под морфо-функциональным резервом понимается вся совокупность структурно-функциональных единиц клетки, органа или ткани, которые в данный момент находятся в состоянии временного покоя, но при необходимости в случаях усиления функциональной активности включаются в работу. В разных органах морфо-функциональный резерв составляет от 60 до 90% всего клеточного состава. Таким образом, благодаря наличию резервных структур клетка или орган при необходимости могут существенно и, что
особенно важно, в самые короткие сроки быстро усилить свою функцию. Следовательно, морфо-функциональный резерв служит для обеспечения быстрого усиления функции клетки, органа или ткани за счёт готовых структур. Используется он в основном для кратковременной компенсации функции. Длительное использование резервных структур приводит к их гиперплазии или гипертрофии. Поскольку болезнь предъявляет повышенные требования к организму, которые выходят за рамки физиологических нагрузок, компенсаторные процессы обычно осуществляются на более мощной морфологической основе. Наиболее ярким примером компенсаторных процессов являются гипертрофия и гиперплазия. Гиперплазия - увеличение количества структурно -функциональных единиц (внутриклеточные органоиды, клетки), сопровождающееся усилением функции органов.
Гипертрофия -увеличение размеров и массы структурно-функциональных единиц (внутриклеточные органоиды, клетки, орган), сопровождающееся усилением их функции. В основе гипертрофии клеток лежит внутриклеточная гиперплазия ультраструктур. В основе гипертрофии органа может лежать как гипертрофия клеток, так и их гиперплазия. Гипертрофия и гиперплазия клеток и тканей обычно возникают после того, как полностью истощится клеточный или тканевой морфо-функциональный резерв. В отличие от морфо-функционального резерва развитие гипертрофии и гиперплазии является основой для долговременной компенсации функции клеток, тканей или органов. Гипертрофия и гиперплазия часто являются основными компонентами структурно-функциональной перестройки органа или ткани. Гипертрофия и гиперплазия тесно связаны с регенерацией и более того развиваются на её основе. Таким образом, гипертрофию клеток можно рассматривать как усиленную внутриклеточную регенерацию, а гиперплазию клеток - как усиленную клеточную регенерацию. Однако гипертрофия и гиперплазия имеют и отличия от регенерации, заключающиеся в том, что при последней функция клетки или органа не усиливается, а только поддерживается на нормальном уровне.
Компенсаторные процессы происходят на внутриклеточном, клеточном, тканевом, органном и организменном уровнях. Внутриклеточный уровень: регенерация, гипертрофия и гиперплазия ультраструктур. Клеточный уровень - регенерация клеток, их гиперплазия, гипертрофия и метаплазия. Тканевой уровень - регенерация, перестройка и метаплазия тканей (жировая ткань в кроветворную и наоборот), организация. Органный уровень - гипертрофия органа (рабочая или викарная), перестройка органа. Организменный уровень - общая атрофия при малокалорийном питании или полном голодании; образование временных функциональных систем.
ЧАСТНЫЕ ФОРМЫ КОМПЕНСАЦИИ ПОСРЕДСТВОМ ГИПЕРТРОФИИ
(компенсаторная гипертрофия).
1. РАБОЧАЯ ГИПЕРТРОФИЯ ОРГАНА
а) гипертрофия скелетной мускулатуры при больших физических нагрузках (в её основе - гипертрофия миоцитов);
б) гипертрофия сердца при артериальной гипертонии или при по роках сердца, гипертрофия стенки мочевого пузыря при аденоме предстательной железы, гипертрофия стенки желудка при рубцовом стенозе привратника (в её основе - гипертрофия мышечных клеток данных органов);
в) гипертрофия селезёнки при сепсисе (в её основе - гиперплазия спленоцитов);
г) гипертрофия миометрия-эндометрия и молочных желез при беременности, связанная со стимулирующим действием эстрогенов и прогестерона (не путать ФОРМЫ компенсации с её МЕХАНИЗМАМИ - нет эндокринной гипертрофии, есть эндокринный механизм рабочей гипертрофии).
2. ВИКАРНАЯ (заместительная) ГИПЕРТРОФИЯ ОРГАНА ИЛИ ТКАНИ. В её основе может быть как клеточная гипертрофия, так и клеточная гиперплазия). а) гипертрофия оставшейся почки, гипертрофия оставшейся части печени после её резекции; б) гипертрофия миокарда вследствие кардиосклероза (напр., постинфарктного).
Понятие о ложной гипертрофии.
Ложная гипертрофия выражается в увеличении массы и размеров органа или ткани, но не сопровождающееся усилением соответствующей функции. К ней относятся:
а) гипертрофические разрастания в виде извращенной регенерации (полипы и кондиломы, гипертрофические разрастания грануляционной ткани в краях хронических язв);
б) пороки развития органов и тканей с их избыточным разрастанием - синдром Паркс-Вебера-Рубашова - гигантомелия при врожденных артерио-венозных свищах; пороки развития сосудов по типу кавернозных гемангиом (гамартии).
в) слоновость при хроническом застое лимфы;
г) при избыточном вакатном ожирении (вследствие атрофии паренхимы молочных желёз, икроножных мышц);
д) при эндокринных дисфункциях (тимомегалия при гипофункции КНП, акромегалия и гигантизм при гиперпродукции СТГ гипофиза, гигантомастия при гиперпродукции пролактина и лактогенного гормона; так называемая железисто-кистозная гиперплазия эндометрия при гиперпродукции эстрогенов);
МЕТАПЛАЗИЯ - представляет собой обратимую трансформацию одного типа клеток в другой внутри одного вида ткани (напр., метаплазия цилиндрического эпителия бронхов в многослойный плоский, метаплазия соединительной ткани в костную или кроветворную). В основе метаплазии лежит изменение дифференцировки общих камбиальных клеток-предшественников. Метаплазия возникает в ответ на длительные патогенные воздействия или изменившиеся условия функционирования клеток и приводит к появлению клеток, более устойчивых к данным патогенным агентам или более адаптированных к выполнению необходимой функции. Поэтому метаплазия представляет собой один из видов долгосрочной адаптивной перестройки тканей. Однако иногда метаплазия может быть результатом спонтанного нарушения дифференцировки камбиальных клеток без видимого адаптивного значения.
Интеграция органов и тканей в разнообразные функциональные ассоциации или системы (т.н. динамичные функциональные системы) в норме как адаптивный процесс наблюдается при воздействии на организм больших физических нагрузок: бег, борьба, поднятие тяжестей. При этом для выполнения этих задач формируется единая общая функциональная система, состоящая не только из скелетной мускулатуры, но и из сердечно-сосудистой, дыхательной и центральной нервной систем.
Интеграция органов и тканей в разнообразные функциональные ассоциации или системы в патологии происходит на всём протяжении заболевания, как в его начале, так и в конце. Причем на смену одной ФС может приходить другая ФС. Например, в терминальном периоде почечной недостаточности в процесс элиминации азотистых шлаков включаются потовые железы, желудочно-кишечный тракт, лёгкие. При этом данные органы вместе с почками формируют единую функциональную систему, выполняющую элиминационную функцию.
6) ДЕКОМПЕНСАЦИЯ - утрата способности к дальнейшей компенсации. Причиной развития декомпенсации является несоответствие степени нагрузки на орган его внутренним возможностям обеспечить необходимый уровень функционирования. Декомпенсация делится на быстро развивающуюся и постепенно развивающуюся.
Морфологические проявления декомпенсации в разных органах в целом однотипны.
Быстро развивающаяся декомпенсация (син. острая недостаточность функции органа или органов) - морфологически характеризуется в основном расстройствами кровообращения в виде стазов, кровоизлияний, отёка, обратимыми дистрофические изменениями. Является в принципе обратимым процессом, так как резервы почти полностью сохранены. Например, в состоянии клинической смерти практически здоровый человек может быть сравнительно легко возвращен к жизни, так как запасы внутриклеточных источников энергии (гликоген, АТФ) ещё велики. Несмотря на свою обратимость, острая декомпенсация тем не менее очень опасна, так как выключение функции органа (например, сердца или почек) происходит быстро и как правило полностью. Постепенно развивающаяся декомпенсация всегда проходит период субкомпенсации (компенсация - cубкомпенсация - декомпенсация). Ее синонимом является хроническая недостаточность функции органа или органов. Морфологически постепенно развивающейся недостаточности свойственны дистрофические, некротические и атрофические изменения, склероз или викарное (вакатное) ожирение. Постепенно развивающаяся декомпенсация обычно является необратимой или труднообратимой, так как все морфо-функциональные резервы клеток уже исчерпаны. Однако из-за длительности развития декомпенсации возможно параллельное развитие компенсаторных изменений, в частности с включением в компенсацию других органов и систем. В результате больной с хронической недостаточностью сердечной деятельности может тем не менее долго жить, хотя и в очень суженном интервале физических нагрузок.
7) АТРОФИЯ - прижизненное уменьшение количества, размеров и массы структурно-функциональных единиц (внутриклеточные органоиды,клетки, орган), сопровождающееся снижением или прекращением их функции. Атрофия обычно сочетается с дистрофическими изменениями клеток и часто ими опосредуется. Атрофия может
быть обратимым процессом, однако при длительном воздействии этиологического фактора атрофия клеток может стать необратимой и перейти в их некроз. Конечной причиной атрофии любого происхождения является ослабление регенераторных процессов в органе и преобладание процессов диссимиляции.
КЛАССИФИКАЦИЯ АТРОФИЙ
ОБЩАЯ МЕСТНАЯ
физиоло- патоло- физиоло- патоло-
гическая гическая гическая гическая
Старение а) Длительное а) атрофия а) вследствие
голодание; желточного длительного
б) Синдром мешка; бездействия;
Симмондса- б) атрофия б) при нарушении
Шихана тимуса кровоснабжения;
в) возрастная в) при длительном
атрофия сдавлении тканей;
мол. желез г) при нарушенной
и гонад иннервации;
д) при нарушенной
гормональной стимуляции.
Физиологическая атрофия - наблюдается на протяжении всей жизни человека: атрофия желточного мешка у эмбриона, боталлова протока, возрастная атрофия тимуса, половых желез, внутренних органов. Основными механизмами возрастной атрофии являются нарушения кровоснабжения органов и тканей, ослабление гормональной стимуляции, общее снижение функциональной активности организма.
Общая атрофия из-за нарушенного питания (кахексия). В первую очередь атрофируются жировые депо, скелетная мускулатуры, затем паренхиматозные органы такие как печень, селезёнка, слизистая ЖКТ. Сердце и мозг получают ввиду этого сравнительно много энергетических субстанций и их атрофия развивается в последнюю очередь.
8) ПЕРЕСТРОЙКА - сложный, комплексный процесс структурно-функциональной адаптации клетки, органа или ткани к изменившимся условиям существования. Возникающие при этом изменения внутренней структуры клеток и органов являются стойкими. Перестройка имеет место как в норме, так и в патологии. Морфологически перестройка представляет собой разнообразные сочетания атрофических процессов, регенерации, гипертрофии,
гиперплазии, метаплазии, организации. Наряду с регенерацией перестройка является важнейшим механизмом адаптации. Структурная перестройка тканей обычно возникает после того как полностью истощается морфо-функциональный резерв данного органа или ткани.
KРИТЕРИИ ТЯЖЕСТИ ПАТОЛОГИЧЕСКИХ ПРОЦЕССОВ.
Степень функциональных расстройств при болезнях зависит от следующих факторов: a) конкретное место развития повреждения (жизненно важный участок или нет); б) обратимость и объем этих изменений; в) быстрота развития патологического процесса. Болезнь протекает наиболее тяжело, если повреждение локализуется в функционально важных отделах органа (например, в проводящей системе сердца), занимает большой объем, представлено быстро протекающими и необратимыми процессами. В этих условиях у организма нет достаточно времени компенсировать функциональные расстройства и смертельный исход болезни является весьма вероятным. Напротив, патологический процесс не является опасным, если процессы повреждения обратимы, занимают не очень большой объем, не локализуются в жизненно важной зоне и развиваются постепенно.
ПОНЯТИЕ О ФУНКЦИОНАЛЬНЫХ И СТРУКТУРНЫХ БОЛЕЗНЯХ.
Единство структуры и функции, подчиняющееся философским категориям единства формы и содержания, сущности и явления, уже априорно выражает неразрывную связь клинического симптома болезни и его морфологического эквивалента. Иными словами, как не существует бесструктурных функций и нефункционирующих структур, так и не существует чисто функциональных расстройств без соответствующих морфологических изменений в органах и бессимптомных структурных изменений. Эти положения можно воспринимать как важнейшие законы патологии. Этим простым логическим анализом доказывается абсурдность утверждений о существовании т.н. функциональных болезней или расстройств и невозможность существования абсолютно бессимптомных (т.н. доклинических) периодов течения болезней. Отсюда вытекают 2 важных практических вывода:
1. Всякий клинический симптом (или симптомы) является результатом конкретных морфологических изменений в клетках или тканях. Эти изменения могут быть невидимыми при световой микроскопии, но они отчётливо региструруются при электронной микроскопии или с помощью гистоферментных методов. Частая обратимость многих патологических симптомов еще не свидетельствует об их "чисто функциональном" происхождении и не должна усыплять бдительность врача. Как минимум, в таких случаях нужно организовать более или менее длительное медицинское наблюдение за больным.
2. Любое заболевание может быть диагностировано на самых ранних этапах своего развития путем активного выявления соответствующих симптомов или специфических маркеров патологического процесса. На самых ранних периодах заболевания его симптомы не отсутствуют, а просто скрыты или трудны для выявления. Большое значение в так называемом бессимптомном течении болезней имеют параллельно развивающиеся компенсаторные процессы, которые сглаживают функциональные расстройства и делают их субъективно не ощутимыми. Исходя из этого врач должен в таких случаях направлять свои усилия на активное выявление скрытых функциональных, морфологических или лабораторных признаков заболевания с целью возможно более ранней его диагностики и своевременного адекватного лечения.
